3A Grubu Elementleri ve Özellikleri
Periyodik tabloda elementler atom numaralarına göre sıralanmıştır. Atom numarası ise atomun çekirdeğindeki proton sayısına eşittir. Periyodik tabloda düşey sütunlara grup denir. Aynı grubun içinde yer alan elementler alt alta dizilmiştir. Bu elementlerin kimyasal özellikleri de benzerdir. Bu yazıda 3A grubu elementleri ve bu elementlerin özellikleri üzerinde duracağız.
Kimyada A grubu elementlerinin önemli olanlarına çeşitli adlar verilmiştir. Örneğin 1A grubuna "alkali metaller", 7A grubuna ise "halojenler" adı verilir. Ancak 3A grubunun özel bir adı yoktur. Buna karşın grubun en üstündeki atom bor olduğu için "bor grubu" olarak da adlandırılır. A ve B gruplarını ayırmadığımız zamanda 3A grubu 13. grup olmaktadır. Bu nedenle grup 13 olarak da karşımıza çıkabilir.
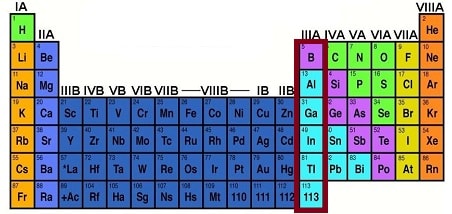
3A grubu elementleri nelerdir? Öncelikle bu gruptaki elementleri adı ve sembolleriyle listeleyim. 3A grubunda şu elementler bulunmaktadır:
- Bor (B)
- Alüminyum (Al)
- Galyum (Ga)
- İndiyum (In)
- Talyum (TI)
3A grubu elementleri için bir kodlama olarak "Bol albümle galip indim tahttan" ifadesini kullanabiliriz.
3A Grubu Elementlerinin Özellikleri
3A grubundaki elementlerin en üstünde bor olduğu için bu grubun özel adı bor grubudur. Periyodik tablonun aynı zamanda 13. grubudur. Alüminyum, galyum, indiyum ve talyum metaliktir. Grubun en üstünde bulunan bor ise yarı metal olarak sınıflandırılır.
3A grubu elementlerinin her birinin elektron konfigürasyonu ns2 np1 ile biter. Yani değerlik elektron sayısı 3'tür. Son s orbitalinde 2 ve son p orbitalinde 1 elektron bulunur. Bu nedenle bileşiklerinde +3 ve +1 arasında değerlik alırlar. Talyum ise daha sabit bir düzen içerindedir ve genellikle +1 değerlik alır. Grup içerisinde genel eğilimler ise şöyledir:
- Atom yarıçapı aşağı doğru artar. (Talyum en büyük atomik yarıçapa sahiptir.)
- Reaktivite aşağı doğru düşer.
- İyonlaşma enerjisi grupta aşağı indikçe azalır.
Aşağıdaki tabloda 3A grubu elementlerinin genel özellikleri verilmiştir.
| Ad | Sembol | Atom numarası | Atom kütlesi (g/mol) | Donma noktası°C | İyonlaşma enerjisi (kJ/mol) |
|---|---|---|---|---|---|
| Bor | B | 5 | 10.8 | 2076 | 801 |
| Alüminyum | Al | 13 | 27 | 660 | 578 |
| Galyum | Ga | 31 | 69.7 | 29.8 | 558 |
| İndiyum | In | 49 | 114.8 | 156 | 558 |
| Talyum | TI | 81 | 205.4 | 303 | 589 |
Yukarıda 3A grubu elementleriyle ilgili genel özellikler tablo halinde verilmiştir.
Kullanım Alanları
3A grubu elementlerinin kullanım alanları üzerinde kısaca duralım. Bu elementlerden yaygın olarak üst sırada yer alan ilk iki element bulunur. Bu elementler bor ve alüminyumdur.
Bor Türkiye'de de maden olarak çok çıkarılan bir yarı metaldir. Çeşitli sanayi ürünlerinin yapısına katılmaktadır. Bazı durumlarda yakıt olarak kullanılmaktadır. Bununla birlikte boraks gibi maddelerin yapısına da katılır.
Alüminyum da çok aktif olarak kullanıla bir metal çeşididir. Metal denince akla gelen ilk elementlerden olmasının sebebi budur. Özellikle sanayide birçok maddenin yapısına alüminyum katılır. Bununla birlikte alüminyum içeren eşyalar hayatımızın her alanındadır.
Galyum elektronik sanayisinde kullanılan bir metaldir. Ayrıca çeşitli optik sürücülerin yapısında da galyum vardır. Kaynama noktasının yüksekliği nedeniyle termometrelerde de kullanılabilir.
İndiyum ve talyumun kullanımı ise daha nadirdir.
3A Grubu Elementlerinin İncelenmesi
Şimdi de bu elementleri tek tek ele alalım.
Bor
Bor, 3A grubunun ilk elementidir ve grubun tek yarı metalidir. Kimyasal sembolü B'dir ve atom numarası 5'tir. Bor [He] 2s22p1 elektron konfigürasyonuna sahiptir ve +3 şeklinde iyonlaşmayı tercih eder. Borun doğal element formu yoktur. Yer kabuğunda bol miktarda bulunan bazı bileşiklerin yapısında bor bulunur.
Bor, bitkiler için vazgeçilmez bir besindir. Boraks olarak bilinen bor cevherlerinin büyük yoğunluklar bulunduğu birkaç yerden biri de Türkiye'dir. Borun oktetini tamamlamamıştır. Bu nedenle bor bir Lewis asididir. En basit olanı diboran olan (B2H6) olan hidritleri oluşturma eğilimindedir. Bor bileşikleri organik bileşikleri sentezlemek için kullanılır. Diğer bor bileşiklerini oluşturmak için kullanılan ana bileşiklerden biri, zayıf bir asit olan ve aşağıdaki iki aşamalı reaksiyonda oluşan borik asittir:
B2O3(k) +3 H2O(s) → 2B(OH)3(aq)
B(OH)3(aq) + 2H2O(s) → H3O+(aq) + B(OH)−4(aq)
Alüminyum
Alüminyum, bor grubunun Al simgesini taşıyan ve atom numarası 13 olan en önemli metalidir. Hafif alaşımlarda kullanılır ve aktif bir metaldir. Elektron konfigürasyonu [Ne] 2s22p1 şeklindedir ve genellikle bir +3 iyon durumunu benimser.
Bu element, Dünya'nın kabuğundaki en bol metaldir (%7.5 - 8.4). Çok bol olmasına rağmen, 1886'dan önce alüminyum değerli bir maden olarak ele alınmaktaydı.Çünkü yüksek erime noktasından dolayı alüminyumu cevherden ayırmak zordu. Alüminyum üretmek için çok pahalıdır, çünkü bir mol alüminyumun elektrolizi üç mol elektron gerektirir.
Al+3 + 3e− → Al(s)
Alüminyum, gümüş veya gri renkli, yumuşak bir metaldir. Son derece reaktiftir ve bu nedenle doğada bileşiklerin yapısında bulunur. Alüminyum su ile reaksiyona girmiyor gibi görünmektedir. Çünkü alüminyum genellikle oksitlenmiş bir Al2O3 tabakası ile korunmaktadır. Bu tabakanın kalınlığı galvanik reaksiyonlara bağlı olarak değişir. Tabakanın varlığı metalin daha fazla oksitlenmesini önler. Bu nedenle birçok yüzeyde paslanmayı önleyici olarak alüminyum kullanılır.
Galyum
Galyumun kimyasal sembolü Ga ve atom numarası 31'dir. Elektron konfigürasyonuna [Ar] 2s22p1 şeklindedir ve +3 iyon durumuna sahiptir. Erime noktası, oda sıcaklığının biraz üzerinde 29.8 ° C'dir. Galyum ikinci en düşük erime noktasına (cıvadan sonra) sahiptir ve sıvı fazda diğer herhangi bir maddeden daha geniş bir sıcaklık aralığında kalabilir.
Galyum endüstriyel olarak önemlidir çünkü ışığı doğrudan elektriğe dönüştüren galyum arsenalini (GaAs) oluşturur. Galyum, hidrojen üretmek için alüminyum ile birlikte kullanılır. Termit reaksiyonuna benzer bir işlemde, alüminyum sudan oksijen çıkarır ve hidrojen gazı salar. Bununla birlikte, yukarıda belirtildiği gibi, alüminyum su varlığında koruyucu bir kaplama oluşturur. Galyum ve alüminyumun birleştirilmesi, bu koruyucu tabakanın oluşumunu engelleyerek, alüminyumun suyu hidrojene indirmesini sağlar.
İndiyum
İndiyum, kimyasal sembolü In ve atom numarası 49 olan bir elementtir. Elektron konfigürasyonuna [Kr] 2s22p1 şeklindedir ve +1 veya +3 iyonlarını oluşturabilir. Bununla birlikte, +3 durumu daha yaygındır. İndiyum galyuma benzeyen yumuşak bir metaldir. İndiyum, optik aygıtlarda fotoiletkenlerde kullanılır.
İndiyumun fiziksel özellikleri arasında gümüş-beyaz rengi ve büküldüğünde ortaya çıkardığı teneke benzeri yapılar vardır. İndiyum asitlerde çözünür, ancak oda sıcaklığında oksijen ile reaksiyona girmez. Çinko cevherlerden ayrılarak elde edilir. İndiyum çoğunlukla alaşım yapmak için kullanılır ve metalik gücü arttırmak için sadece küçük bir miktarı yeterlidir. Örneğin, metalleri daha kullanışlı endüstriyel aletler yapmak için altın veya platine indiyum eklenir.
Talyum
Talyum, Tl sembolü ve atom numarası 81 olan bir elementtir. Elektron konfigürasyonu [Xe] 2s22p1 şeklindedir ve +3 veya +1 oksidasyon durumuna sahiptir. Yukarıda belirtildiği gibi, talyum ağır olduğu için +1 yüklenmesi daha yaygındır. Talyum yumuşak ve zehirlidir. Bununla birlikte yüksek sıcaklıklı süperiletkenlerde kullanılır. Zehirli etkisinden dolayı kullanımı zamanla yasaklansa da daha önceleri talyum fare zehirlerinde kullanılmıştır.
Etiketler:
Son Eklenenler
- Tarımla İlgili Meslekler
- Matematiği İyi Olmayanlar Hangi Mesleği Seçmeli?
- Antropoloji Nedir?
- Dünyanın Kaç Türlü Hareketi Vardır?
- Toplumsal Düzeni Sağlayan Kurallar Nelerdir?
- Cumhuriyet Yönetiminin Değerleri Nelerdir?
- İklim ve Hava Olayları Arasındaki Fark
- 1 Asal Sayı Mıdır?
- Homeostasi nedir?
- 2 ile Bölünebilme Kuralı
