Karışım Nedir?
Karışım kavramı 4. sınıf fen dersinden itibaren karşımıza çıkan bir kavramdır. Bu yazıda karışım nedir sorusunu kısaca yanıtlamaya çalışacağız. Öncelikle şunu belirtmek gerekir ki maddeler saf madde ve karışımlar olarak ikiye ayrılır. Doğal olarak saf olmayan maddelerin tamamı karışımdır.
Demek ki iki madde bir araya geldiğinde ya arada kimyasal reaksiyon gerçekleşir ya da bu maddeler karışım oluşturur. Karışımlarda kimyasal değişim olmaz. Bu nedenle fiziksel yöntemlerle karışımlar bileşenlerine ayrışabilirler.
Karışımların Özellikleri
Karışım nedir kısaca öğrendik. Şimdi de karışımların özellikleri üzerinde biraz duralım. Karışımların özellikleri maddeler halinde şöyle özetlenebilir.
- İki veya daha fazla saf maddenin bir araya gelmesiyle oluşurlar.
- Sembol veya formül şeklinde ifadelerle gösterilemezler.
- İçerisinde birden fazla element veya bileşik bulunur.
- Karışıma katılan maddeler arasında sabit bir oran yoktur.
- Karışım sonucu kimyasal tepkime gerçekleşmez ve kimyasal özellikler değişmez.
- Karışımlar fiziksel yöntemlerle bileşenlerine ayrılabilir.
- Karışımdaki bileşenler kendi özelliklerini muhafaza eder.
- Saf madde olmadıkları için saf maddelere ait bazı özellikleri göstermezler.
- Erime, kaynama noktaları gibi ayırt edici özellikleri yoktur.
- Hal değişimi sırasında sıcaklıları sabit değildir.
Karışımlar Kaça Ayrılır?
Karışımların sınıflandırılması da önemlidir. Karışımları temel olarak ikiye ayırırız.
- Homojen karışımlar
- Heterojen karışımlar
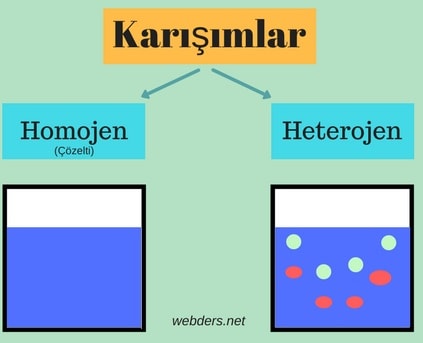
Homojen Karışım Nedir?
Homojen bir karışım, kolayca ayrılmayan düzenli bir bileşime sahiptir. Homojen bir karışımın her tarafı aynı görüntüye ve özelliklere sahiptir. Homojen bir karışımda, tipik olarak bir çözünen ve bir çözücü bulunur ve ortaya çıkan madde, tek bir fazdan oluşur. Homojen karışım için en yaygın örnek suda çözünen tuzla elde edilen tuzlu su karışımıdır.
Homojen bir karışım herhangi bir sayıda bileşen içerebilir. Tuzlu su çözeltisi sadece su (çözücü) ve tuz (çözücü) içerirken, hava birçok gaz içerir. Havada çözünenler arasında oksijen, karbondioksit ve su buharı bulunur. Havadaki ana çözücü ise azottur.
Heterojen Karışım Nedir?
Homojen karışımların aksine heterojen karışım, tek tip özellik sergilemez. Karışımdaki partikülleri görmek ve birbirinden ayırmak genellikle mümkündür. Heterojen karışımların örnekleri arasında ıslak sünger, kum, çakıl, ve su tebeşir tozu karışımı bulunur.
Heterojen karışımları çözelti dışında kalan bütün karışımlardır. Günlük hayatta birçok heterojen karışım örneğine rastlarız.
Şöyle bir örnek verelim. Suya tuz attığımızda tuzun çözünmesiyle oluşan tuzlu su bir homojen karışımdır. Ancak suya çok fazla tuz atarsak ve dipte tuz çökelti olarak kalırsa bu durumda heterojen karışım elde edilir. Çünkü dipteki tuz gözle bile görülebilmektedir.
Heterojen karışımlar da çeşitli şekilde sınıflandırılır.
Süspansiyon: Katı ve sıvıların karıştırılmasıyla elde edilir. Su tebeşir tozu, su ve kum karışımı, yediğimiz sulu yemekler süspansiyon örnekleridir.
Emülsiyon: Bir sıvının başka bir sıvıyla yaptığı karışımdır. Örneğin zeytinyağı su karışımı en yaygın emülsiyon örneğidir. Zeytinyağı suda çözünmez ve daha hafif olduğu için üstte birikir. Mazot ile su karışımı da yine emülsiyon örneğidir.
Kolloid: Çözeltiye benzemekle birlikte aslında çözelti olmayan heterojen karışımlardır. Örneğin ayran bu özelliğe sahiptir. Yine süt ve kan gibi maddelere dışarıdan bakarsanız tek tip görünürler ancak bunlar çözelti değildir. Yani heterojen karışımdır.
Aerosol: Katı ya da sıvı maddelerin gaz içerisine girerek oluşturduğu karışımlardır. Örneğin sis ve duman birer aerosol örneğidir.
Etiketler:
Son Eklenenler
- Tarımla İlgili Meslekler
- Matematiği İyi Olmayanlar Hangi Mesleği Seçmeli?
- Antropoloji Nedir?
- Dünyanın Kaç Türlü Hareketi Vardır?
- Toplumsal Düzeni Sağlayan Kurallar Nelerdir?
- Cumhuriyet Yönetiminin Değerleri Nelerdir?
- İklim ve Hava Olayları Arasındaki Fark
- 1 Asal Sayı Mıdır?
- Homeostasi nedir?
- 2 ile Bölünebilme Kuralı
