Atom Yarıçapı
Atomun küresel yapıda olduğu bilinmektedir. Bu nedenle atom hacmi için en temel ölçüt atom yarıçapıdır.
Atomik yarıçap, atomların çeşitli fiziksel ve kimyasal özellikleri gibi birçok yönünü belirlemek için kullanılır. Periyodik tablo, atom yarıçapını belirlemeye büyük ölçüde yardımcı olur ve bir dizi eğilim sunar.
Bu yazıyı bitirdiğinizde atom yarıçapı ve iyon yarıçapı ile ilgili bilmeniz gereken her şeyi öğreneceksiniz. Ardından vereceğimiz örneklerle konuyu pekiştirme imkânı bulacaksınız.
Öncelikte şunu hatırlatalım. Yarıçap çapın yarısı demektir. Bu nedenle atom yarıçapı ile atom çapı paralel kavramlardır.
Atom Yarıçapı Nasıl Değişir?
Atom yarıçapı bizim için elementlerin özelliklerini kıyaslama açısından bilgiler sunar. Bu nedenle atom yarıçapı periyodik tabloda nasıl değişir bilmek durumundayız.
Şunu belirtelim ki normalde atom sayısı büyük olan atomların daha geniş çapa sahip olması gerekir. Çünkü daha büyük atom çapı daha çok elektron demektir. Ancak örnekleri incelediğimizde bu durumun böyle olmadığını görüyoruz.
Atom numarası büyüdüğünde eğer elektronlar yeni bir yörünge oluşturmuşsa çap büyüyecektir. Ancak eşit sayıdaki yörüngede elektron sayısı az olanın çapı daha büyük olacaktır. Eşit sayıda yörünge demek aynı periyotta yer almak demektir.
Atom Yarıçapı Karşılaştırma
Yukarıdaki bilgiler size karışık geldiyse doğrudan karşılaştırma yöntemiyle konuyu kavramaya çalışın. Atom yarıçapı kıyaslanırken önce periyota bakılır. Periyot numarası ile yörünge sayısı zaten paraleldir. Bu nedenle periyot numarası büyük olan atomun yarıçapı daha büyük olur.
Yani 4. periyotta bulunan atomların yarıçapları elbette 3. Periyottaki atomlardan daha fazladır. Çünkü atomların çevresinde daha çok elektron yörüngesi oluşmuştur.
Burada karışıklık aynı periyotta atomları karşılaştırmaktan kaynaklanmaktadır. Aynı periyotta sol tarafta atom yarıçapları daha büyüktür. Çünkü yörünge sayıları eşit olduğunda az proton daha büyük çap demektir. Protonlar + yüklü olduğunda elektronları daha çok merkeze çekecektir.
Örneğin aynı periyotta yer alan Na ve Al elementlerinden Na’nın atom numarası 11, Al’in ise 13’tür. Bu durumda Al’in atom numarası büyük olmasına rağmen Na elementi daha geniş yarıçapa sahiptir.
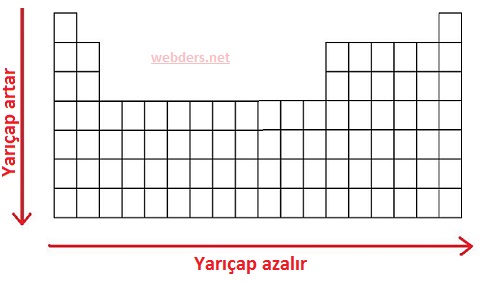
Yukarıdaki görselde atom yarıçapının periyodik sistemdeki değişimi gösterilmektedir. Bu görsel bütün konuyu özetlemektedir.
İyon Yarıçapı
Buraya kadar anlattıklarımız nötr atomlarla ilgiliydi. Şimdi ise iyonları ele alalım.
Elektron almış ya da vermiş atoma iyon denir. İyon yarıçapı kıyaslarken aynı atomun farklı iyonları arasında kıyaslama yapılabilir.
Eğer farklı iyonların atom numaraları arasında kıyaslama yapılacaksa elbette periyodik tablodaki yer baz alınacaktır.
Aynı atomun iyon yarıçapı karşılaştırması yapıldığında elektron sayısı çok olanın bu sefer çapı büyük olacaktır. Çünkü aynı atomun proton sayısı eşit olacaktır. Bu durumda daha az elektron demek merkeze daha fazla çekilmek demektir.
Örneğin K atomunun çapı K+2 iyonundan daha büyüktür. Çünkü 2 elektron veren iyonda elektron sayısı proton sayısının altına düşmüştür. Bu durumda elektron başına düşen çekim kuvvet artmış ve çap azalmıştır.
Konu aslında çok basit olmasına rağmen anlaşılmadığında çok karıştırılmaktadır. Bu nedenle aşağıdaki örnekleri incelemeniz çok önemlidir. Eğer örnekleri anlarsanız konuyu da iyi anlamışsınız demektir.
Atom ve İyon Yarıçapı ile İlgili Sorular
- Aynı periyotta yer alan atom numarası 26 olan A atomu ve atom numarası 28 olan B atomundan hangisinin yarıçapı büyüktür?
- 4. Periyotta yer alan X atomu ile 3. Periyotta yer alan Y atomundan hangisinin yarıçapı büyüktür?
- K, K+ ve K- atom ve iyonlarının yarıçaplarını büyükten küçüğe sıralayın.
- Na+ iyonu ve nötr Ne atomunun elektron sayıları eşittir. Hangisinin yarıçapı büyüktür?
- Periyodik tabloda yarıçapın büyük olması için aşağıda olmak mı önce gelir yoksa solda olmak mı?
Cevaplar
- A
- X
- K- > K > K+
- Na+
- Aşağıda olmak
Cevaplarda en ufak bir tereddüt gösterirseniz yukarıdaki ilgili kısmı tekrar okumayı ihmal etmeyin.
Etiketler:
Son Eklenenler
- Tarımla İlgili Meslekler
- Matematiği İyi Olmayanlar Hangi Mesleği Seçmeli?
- Antropoloji Nedir?
- Dünyanın Kaç Türlü Hareketi Vardır?
- Toplumsal Düzeni Sağlayan Kurallar Nelerdir?
- Cumhuriyet Yönetiminin Değerleri Nelerdir?
- İklim ve Hava Olayları Arasındaki Fark
- 1 Asal Sayı Mıdır?
- Homeostasi nedir?
- 2 ile Bölünebilme Kuralı
