Azot Oksit (NO) Bileşiği
Azot oksit bileşiği NO formülüne sahip bir kimyasal bileşiktir. Bileşikler konusu içerisinde nötr oksit sınıfında incelenir. Nötr oksitler 3 tanedir. Bunlar NO, NO2 ve CO bileşikleridir. NO bileşiği iki ametal olan Azot (N) ve Oksijenin (O) bir araya gelmesiyle oluşmuştur. Ametaller arasında oluşan bir bileşik olduğu için kovalent bağlıdır.
NO ametal oksidi olduğu için azot monoksit olarak da adlandırılabilir. Aynı mantıkla NO2 azot dioksit olarak adlandırılır.
Azotun oksijenle yaptığı oksit bileşiklerinden en sade olanıdır. NO bileşiği dışında da iki elementin oluşturduğu birçok bileşik bulunmaktadır.
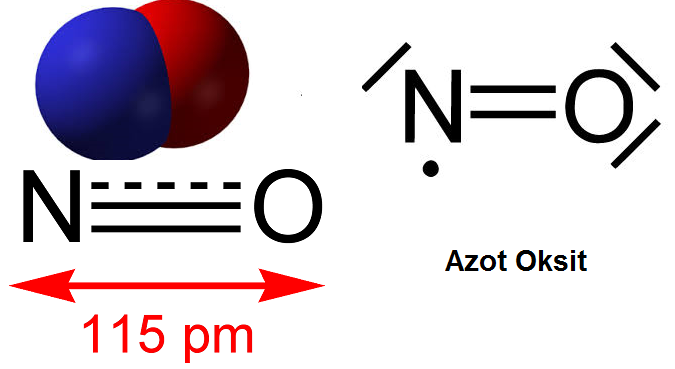
NO Özellikleri
NO oda koşulları altında gaz yapıda renksiz bir bileşiktir. Bağ yapısı eşleştirilmemiş bir adet elektron bulundurur. Bu da molekülün gösteriminde azotun altında veya üstünde bir nokta olarak gösterilir. İki atomdan oluşan moleküllere diatomik moleküller denir. NO bileşiği de bu sınıf içerisinde yer alır.
İnsanlar dahi birçok memelide azot oksit önemli bir hücre uyarıcısıdır. Fizyolojik ve patolojik birçok süreçte azot oksit hücre uyarıcısı olarak rol alır.
NO Tepkimeleri
Azot oksit oksijenle temas ettirildiğinde azot dioksit molekülü ortaya çıkar. Tepkime şöyle gerçekleşir:
2NO + O2 → 2NO2
Azot okside su ve oksijen eklendiğinde nitrik asit meydana gelir. Tepkime şöyledir:
4NO + O2 + 2H2O → 4HNO2
NO aynı zamanda flor, klor, brom gibi halojenlerle tepkime verir. Böylece molekül yapısına üçüncü bir ametal dahil olur.
2NO + Br2 → 2NOBr
NO Elde Edilmesi
NO bileşiğini elde etmek için birden farklı yöntem bulunur. Amonyağı yüksek sıcaklıkta oksijenle tepkimeye sokarsanız su ile birlikte azot oksit de elde edersiniz. Bu tepkime platin katalizörlüğünde gerçekleşir.
4NH3 + 5O2 → 4NO + 6H2O
Element olarak bulunan O2 ve N2’den de NO bileşiği çok yüksek sıcaklıklarda elde edilir.
N2 + O2 → 2NO
Bu yöntemlerin dışında HNO3’ün bakırla tepkimesinden ya da alkali metal azot dioksit bileşiklerinin çeşitli bileşiklerle tepkimeye girmesinden elde edilebilir.
NO bileşiği polar kovelent bağlıdır. İki elementin çekim kuvvetinin farklı olması kutuplu yapıyı ortaya çıkarmıştır. Bu bileşikle ilgili akılda tutulması gereken diğer önemli bir özellik de nötr oksit sınıfından olmasıdır. Nötr oksitler oksijence fakir oksitlerdir.
Etiketler:
Son Eklenenler
- Tarımla İlgili Meslekler
- Matematiği İyi Olmayanlar Hangi Mesleği Seçmeli?
- Antropoloji Nedir?
- Dünyanın Kaç Türlü Hareketi Vardır?
- Toplumsal Düzeni Sağlayan Kurallar Nelerdir?
- Cumhuriyet Yönetiminin Değerleri Nelerdir?
- İklim ve Hava Olayları Arasındaki Fark
- 1 Asal Sayı Mıdır?
- Homeostasi nedir?
- 2 ile Bölünebilme Kuralı
